Antecedentes históricos
El término “parálisis cerebral” (PC) tiene su origen en 1862 cuando William John Little, un cirujano ortopedista inglés, presentó sus observaciones en un grupo de niños con alteraciones del tono y el desarrollo que él describió como “rigidez espástica”. Notó que muchos de estos niños tenían antecedentes de trabajo de parto prolongado, difícil o presentación distócica, postulando que los trastornos motores observados en estos niños eran resultado de trastornos en el proceso del nacimiento.
Esta idea fue aceptada durante alrededor de un siglo.
En 1897 el neurólogo Sigmund Freud planteó en su obra “Parálisis cerebral” que estas dificultades perinatales eran resultado de anormalidades preexistentes en el feto más que la causa misma de la parálisis cerebral (1).
Definición
El término PC define a un grupo de trastornos del control del movimiento y la postura, no progresivos, que ocurren por una injuria sostenida en etapas precoces del desarrollo del sistema nervioso, esto es dentro de los primeros 5 años de vida (2).
Las características esenciales de este síndrome son:
- Es un trastorno de predominio motor (si bien puede acompañarse de otros déficits o anormalidades)
- La lesión no es progresiva (pero sus manifestaciones pueden experimentar cambios con relación al crecimiento y desarrollo del niño; y sin intervenciones apropiadas de neurorrehabilitación puede producirse deterioro músculo esquelético y/o funcional a mediano o largo plazo).
- La localización de la alteración es cerebral, sobre el foramen magno.
- Ocurre en etapas de crecimiento acelerado del cerebro, periodo que para algunos concluye a los 3 y otros a los 5 años en que se estima completado un 95% del cerebro. (3)
- Debe excluirse una enfermedad progresiva del sistema nervioso central.
Pese a ser considerada una encefalopatía estática, derivada de una lesión no progresiva , sus manifestaciones , es decir, las alteraciones del tono y la postura pueden cambiar en circunstancias relacionadas al crecimiento y desarrollo del niño.
Esta entidad es separada de otros cuadros neurológicos por razones diagnósticas y terapéuticas: en primer lugar porque requiere un diagnóstico etiológico lo más exacto posible y una revisión permanente del diagnóstico a fin de excluir trastornos progresivos y en segundo lugar porque implica una aproximación de tratamiento y manejo en múltiples áreas, esto es tratamiento del trastorno motor y los déficits asociados, educación, servicio social, etc. (4).
Epidemiología
Se ha estimado una incidencia mundial de PC de 2 a 2,5 por 1000 recién nacidos vivos con escasa variación entre países desarrollados y leve mayor frecuencia en países en desarrollo. (5) La prevalencia de PC no ha cambiado significativamente en el tiempo y por el contrario se observa un aumento en décadas (1970 y 1990) atribuido al mejor manejo neonatológico que permite la sobrevida de niños con factores de riesgo prenatal de PC y/o de muy bajo peso con alto riesgo de PC. (6, 7).
Etiologías en Parálisis Cerebral
Entre 1959 y 1966 el Proyecto Nacional Perinatal Colaborativo siguió a 56.0000 mujeres embarazadas y sus hijos durante 7 años, a fin de determinar los factores causales de parálisis cerebral. Este estudio prospectivo multicéntrico sigue siendo el estudio más importante en la investigación de la asociación entre la asfixia perinatal y secuelas en el desarrollo neurológico, en particular la parálisis cerebral, sin embargo esta asociación sigue siendo motivo de controversia.
Dentro de las conclusiones del proyecto colaborativo, destaca que el 0,5% de los niños desarrolló PC, siendo los factores principales el bajo peso de nacimiento (<1500 grs.) y la asfixia perinatal. La parálisis cerebral no se desarrolló en la mayoría de los neonatos de término con asfixia con un puntaje de Apgar < 3 a los 5 minutos, pero se definió una prevalencia de aproximadamente 60% de parálisis cerebral en los sobrevivientes de término con puntajes de Apgar ≤ 3 a los 20 minutos. Muchos de los niños con asfixia severa tenían anomalías cerebrales congénitas, de modo que la asfixia como hecho aislado solo daba cuenta del 10% de los casos de PC. (8, 9) En este estudio no se incluyeron factores de riesgo que actualmente se han asociado a PC como trombofilia materna o fetal (10), infección materna o corioamnionitis (11) y embarazos múltiples. (12).
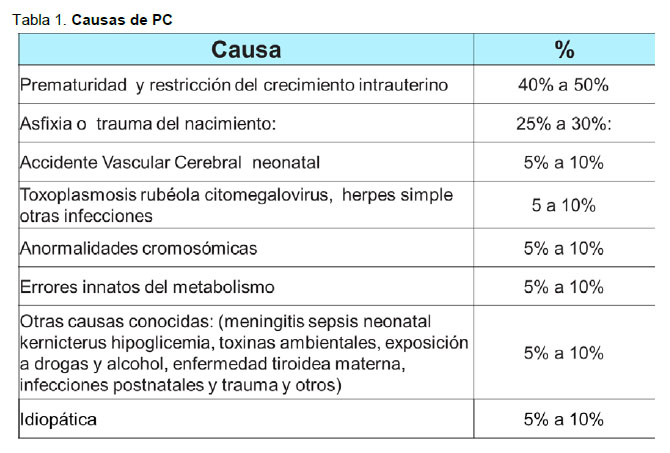
En la medida que se plantean criterios más estrictos para definir una asfixia neonatal, la contribución de ésta a la parálisis cerebral se reduce. Los criterios más estrictos son los propuestos por el Colegio Americano de Ginecólogos y Obstetras para Encefalopatía Neonatal y Parálisis Cerebral. Se ha planteado que el uso de tales estrictos criterios puede subestimar los riesgos de parálisis cerebral posterior a la asfixia del nacimiento. Hermansen en la editorial de Clinics in Perinatology 2006, dedicada al tema, realiza una estimación de la contribución de cada causa en la población total de pacientes con parálisis cerebral (Tabla 1) (13).
Patogenia de la lesión cerebral que da origen a una PC
Desde el punto de vista fisiopatológico, la injuria cerebral afecta grupos de neuronas en áreas primarias del control motor (sistema piramidal) o centros moduladores del movimiento (sistema extrapiramidal y cerebelo), pudiendo afectar además áreas cerebrales no relacionadas directamente al control motor lo que da cuenta de las deficiencias asociadas. El compromiso de estos grupos de neuronas determina deterioro de movimiento o movimientos involuntarios y falta del control inhibitorio que ejercen sobre las motoneuronas en la médula espinal.
Clínicamente, la injuria neuronal determina déficit o anormalidades en el control motor, movimientos involuntarios (distonía, diskinesias), temblor y/o espasticidad. La variable combinación de estos síntomas y signos explica la gran diversidad de manifestaciones que caracteriza a los pacientes con PC.
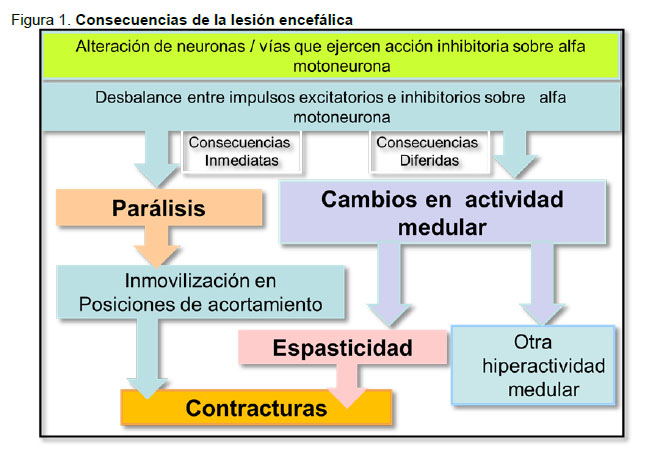
La lesión cerebral que da origen a una parálisis cerebral implica una alteración de las neuronaso vías motoras que ejercen una acción inhibitoria sobre la alfa motoneurona del asta anterior de la médula espinal, con un desbalance entre los impulsos excitatorios e inhibitorios que se ejercen sobre ésta, lo que genera consecuencias inmediatas como el déficit motor derivado de la lesión de neuronas motoras y consecuencias diferidas derivadas de los cambios en la actividad medular con un aumento de tono (espasticidad). Déficit motor y espasticidad contribuyen a la reducción de rangos articulares o contracturas (Figura 1).
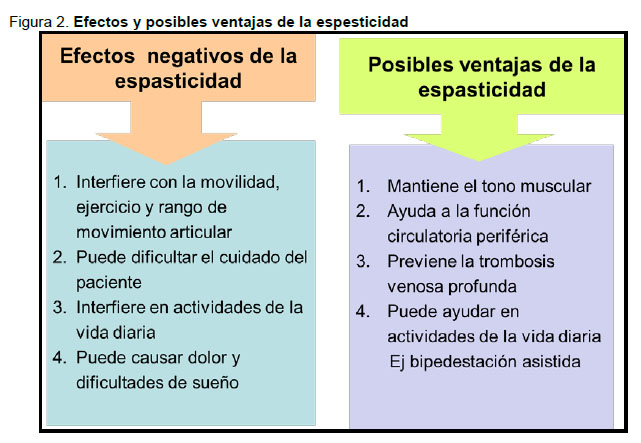
La espasticidad tiene consecuencias en su mayoría negativas. Sin embargo existen algunas posibles ventajas de la espasticidad, señaladas en la Figura 2.
Clasificación de las PC según síntomas y signos predominantes y topografía
Los tipos de PC se diferencian según el segmento corporal comprometido y los síntomas y signos motores predominantes:(14, 15).
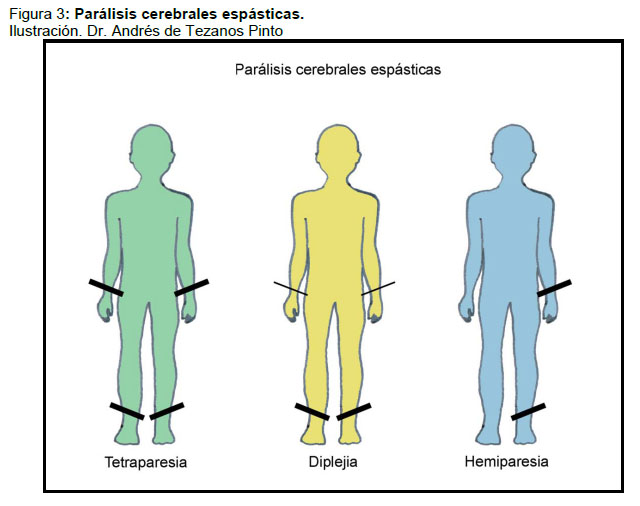
- Parálisis cerebral espástica: predominan los signos piramidales y según su distribución topográfica se clasifica en: (Figura 3)
- Hemipléjica: se considerala forma más frecuente de PC espástica, (20 a 40 % de las PC). Se caracteriza por compromiso piramidal de un hemicuerpo, generalmente con mayor compromiso de la extremidad superior Es frecuente lahipotrofia de las extremidades paréticas, desarrollo cognitivo normal o cercano a lo normal y riesgo de epilepsia que alcanza al 50% en algunas series publicadas.
- Diplejia espástica: Constituye aproximadamente el 20%, (10 a 33%) de las PC: Existe compromiso piramidal de las 4 extremidades, en mayor grado de las inferiores y se relaciona con antecedente de prematuridad.
- Cuadriplejia o tetraparesia: Caracterizada por compromiso armónico de las 4 extremidades, constituye cerca del 27%, de las PC. Se asocia frecuentemente a compromiso cognitivo, déficit sensoriales, epilepsia y sindrome pseudobulbar.
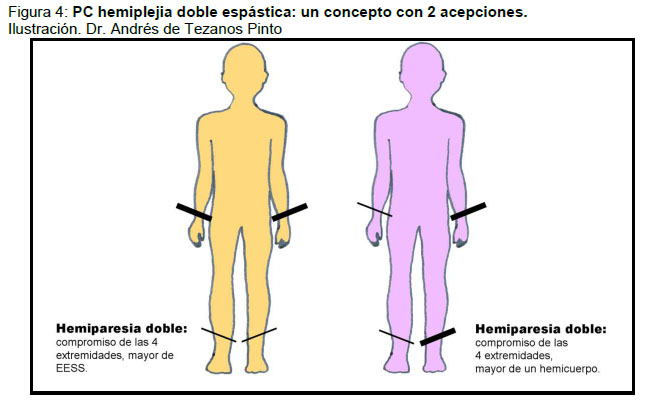
- Hemiplejia doble espástica: concepto en desuso, se refiere a compromiso motor de las 4 extremidades, sin embargo para algunos el concepto implica compromiso mayor extremidades superiores, y para otros mayor de un hemicuerpo.(Figura 4). Constituye una forma más grave, habitualmente asociada a compromiso cognitivo severo.
- Parálisis cerebral extrapiramidal o diskinética: predominan los movimientos anormales (corea /atetosis o distonía) con alteración del tono y la postura (13%, 9-22% de las PC).
- Parálisis cerebral mixta: asocia síntomas piramidales con extrapiramidales (20%)
- Parálisis cerebral atáxica: predomina la ataxia e hipotonía que se mantiene en el tiempo. Puede observarse en niños que sufren injuria predominantemente a nivel cerebeloso .Requiere un exhaustivo estudio de diagnóstico diferencial tendiente a descartar enfermedades progresivas.
- Parálisis cerebral hipotónica: muy poco frecuente, se discute su valor como entidad separada,
Las PC se clasifican de acuerdo al gradode limitación funcional en actividades de la vida diaria en “leve”, sin limitaciones, “moderada”, con algunas limitaciones y “severa”, con importante limitación en la realización de todas las actividades de la vida diaria.(16)
En general la evolución de las PC es hacia la adquisición de habilidades motoras, cognitivas y de lenguaje, aunque de modo más lento y muchas veces incompleto, que en un niño sin este cuadro. El nivel de adquisición de habilidades dependerá del tipo de PC y del grado de compromiso encefálico como también de los déficits asociados. Los niños hemipléjicos, adquieren la marcha hacia los 2 años, en tanto que en las diplejias espásticas en más del 50% se logra hacia los 3 años(17).
Enfoque diagnóstico en PC
El diagnóstico de PC es clínico. Los estudios complementarios tienen como finalidad identificar la causa cuando ésta no es evidente por la historia clínica, determinar magnitud y localización del daño (neuroimágenes), descartar causas progresivas (enfermedades neurometabólicas o neurodegenerativas) y detectar trastornos asociados y/o complicaciones (18).
El diagnóstico precoz es fundamental para iniciar tratamiento en forma oportuna, para lo cual es necesario identificar a niños de alto riesgo:
- Perinatales: Prematurez, antecedentes de asfixia perinatal, restricción de crecimiento intrauterino,etc.
- Desarrollo Temprano: letargia, irritabilidad, pobre control cefálico, succión débil, postura hipertónica, protrusión lingual, hipersensibilidad oral, bajo interés por el medio, movimientos anormales.
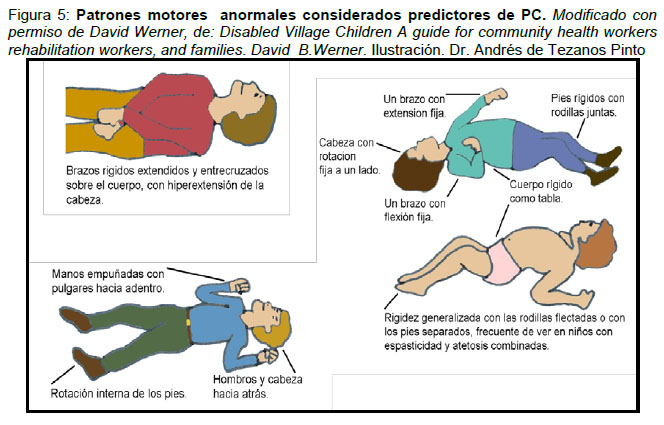
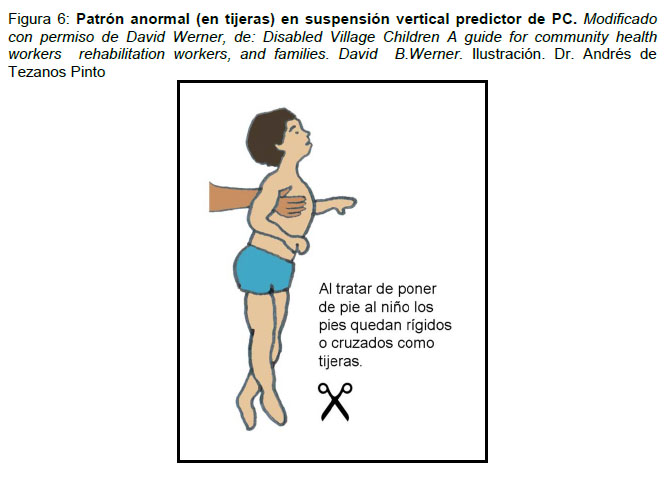
- Manifestación temprana de patrones motores anormales que se consideran predictores de PC. (19) ( Figura 5 y 6)
- Retraso en hitos del desarrollo psicomotor.
Diagnóstico diferencial
El diagnóstico de PC es un diagnóstico sindromático, y requiere la exclusión de patologías progresivas, por lo que en cada niño es necesario plantear la posibilidad de otras condiciones neurológicas como lesiones encefálicas ocupantes de espacio, trastornos neurodegenerativos, lesiones de la médula espinal, enfermedades neuromusculares y errores innatos del metabolismo. Aun cuando la evaluación inicial no sugiera cuadros progresivos, en la evolución posterior es necesario reconsiderar periódicamente el diagnóstico de PC ya que las alteraciones neuroimagenológicas en enfermedades neurometabólicas o neurodegenerativas no siempre son evidentes en etapas precoces de la enfermedad. Un ejemplo es el déficit de pantotenatokinasa, trastorno del metabolismo del fierro que se manifiesta por compromiso motor de curso muy lentamente progresivo, de difícil pesquisa.
En este trastorno del metabolismo se produce depósito de fierro en ganglios basales con gliosis, que en etapas precoces de la enfermedad puede no ser evidente, apareciendo posteriormente la imagen característica de depósito de fierro y gliosis en el globo pálido, llamada “en ojos de tigre”.
Reforzando lo anterior, todo niño con un trastorno motor crónico requiere un análisis exhaustivo tendiente a:
- Identificar la posible patogenia
- Objetivar y registrar las características del compromiso motor y del estado funcional periódicamente para pesquisar progresión del déficit motor, aparición de nuevos síntomas, signos y/o alteraciones neuro-imagenológicas que obligan a reconsiderar
- Definir diagnóstico,planteando posibles causas progresivas y/o tratables, tomando en consideración datos epidemiológicos e incidencia de enfermedades a cada edad en particular.
Este proceso de análisis y diagnóstico diferencial es imprescindible para planificar el tratamiento y se realiza mediante:
- Anamnesis repetida, definiendo perfil temporal de signos y síntomas, definiendo orden o edades de aparición de síntomas y signos. Evaluar fluctuaciones del compromiso motor: Trastornos motores fluctuantes en el día pueden corresponder a Distonía respondedora a L- Dopa, entidad tratable que puede ser confundida con una Parálisis Cerebral.
- Búsqueda dirigida de antecedentes familiares: enfermedades neurológicas o compromiso multisistémico en trastornos neuro-metabólicos, presencia de consanguinidad. Enfermedades hereditarias autosómica recesivas, pueden ser difíciles de demostrar en familias pequeñas o en que la genealogía sea incompleta. .
- El examen físico y neurológico realizado a distintas horas del día permite advertir fluctuaciones diurnas. La aplicación de escalas funcionales y/o de logro de actividades de la vida diaria son de utilidad para detectar cambios no relacionados a inmovilidad, crecimiento o complicaciones de la parálisis cerebral.
Trastornos asociados en Parálisis Cerebral: (20)
- Déficit intelectual (DI), alrededor del 50% de las personas afectadas presenta algún grado de DI. Los portadores de PC extrapiramidales tienen mejor nivel intelectual, y aquellos con tetraparesia espástica cursan con déficit intelectual más severo.
- Epilepsia: 25 a 30% tienen epilepsia de diferentes tipos y de inicio en general dentro de los primeros dos años de vida; es más frecuente en niños con PC hemipléjica y cuadripléjica y en los con mayor déficit intelectual.
- Déficit visual: afecta al 50% de los niños con PC. Su severidad se asocia a la del trastorno motor y mental. La anomalía más frecuente es la falta de control de los movimientos oculares con estrabismo. Otras alteraciones son la ambliopía, atrofia óptica, hemianopsias, vicios de refracción y los defectos propios de la patología de base (cataratas, coriorretinitis etc.).
- Déficit auditivo: Se presenta en alrededor de 10 a 15 % de las PC, más frecuente en portadores de PC extrapiramidal secundaria a kernicterus o encefalopatía bilirrubínica en hijos de madres Rh negativas no inmunizadas, patología que se ha hecho infrecuente. Actualmente se relaciona con casos de incompatibilidad de grupo clásico o Encefalopatía Hipóxico Isquémica con compromiso de ganglios de la base.
- Trastornos del lenguaje y del habla: debidos a factores motores, intelectuales, auditivos y ambientales. Los trastornos del habla, dispraxia verbal, anartria y disartria son frecuentes en portadores de PC extrapiramidales, siendo importante detectar signos de intención comunicativa e implementar técnicas de comunicación aumentativa/ alternativa (CAA). Los trastornos del lenguaje en niños con PC (disfasias semánticas, semántico-pragmáticas, y fonológico-sintácticas)requieren alto grado de sospecha así como terapeutas de lenguaje capacitados en identificar estos trastornos y proporcionar las alternativas terapéuticas que ofrezcan mayor funcionalidad en la comunicación del niño.
- Trastornos de Aprendizaje: Educadores diferenciales con experiencia en educación de niños con discapacidad motora en colaboración con terapeutas de lenguaje pueden detectar trastornos específicos de aprendizaje como dislexia y/o discalculia e implementar intervenciones que permitan minimizar las repercusiones de estas dificultades en el aprendizaje global del niño. Educadores deben capacitarse para asumir los procesos de integración a escolaridad regular en los niños habilitados para hacerlo.
- Trastornos del sueño: frecuentes en pacientes con PC, requieren manejo con estrategias de hábito de sueño y eventualmente uso de fármacos reguladores del ciclo sueño- vigilia.
- Trastornos psiquiátricos: Los trastornos de conducta con auto o hétero-agresión son motivo de consulta frecuente, que requieren manejo farmacológico cuidadoso, puesto que el uso de tranquilizantes neurolépticos pueden exacerbar movimientos anormales incluso tras su suspensión. Trastornos del ánimo pueden manifestarse en pacientes muy discapacitados con buen potencial intelectual, especialmente hacia la adolescencia en que se hacen conscientes de sus déficits y limitaciones. Otros trastornos psiquiátricos también pueden ocurrir en pacientes con PC, incluyendo trastornos bipolares o psicosis, lo que pudiera ser provocado por uso de algunos fármacos. La disfunción familiar asociada a enfermedad crónica, invalidante y de alto costo, suele afectar a la familia completa y se debe abordar con intervenciones a nivel familiar.
Complicaciones de la Parálisis Cerebral Las complicaciones de la PC comprometen distintos sistemas y pueden afectar significativamente la calidad de vida del niño y su familia. Entre ellas destacan como las más frecuentes:
- Ortopédicas: contracturas músculo-esqueléticas, luxación de cadera, escoliosis, osteopenia y fracturas patológicas.
- Problemas digestivos: reflujo gastroesofágico, dificultades para la alimentación, desnutrición, constipación)
- Problemas respiratorios: hipersecreción bronquial persistente, tos crónica, neumonías, aspiración
- Alteraciones buco-dentales, alteraciones cutáneas, vasculares y diferentes problemas que pueden provocar dolor y molestias.
Estas complicaciones están frecuentemente relacionadas: la presencia de reflujo gastroesofágico e incoordinación faríngea debido a factores mecánicos y neurológicos (síndrome pseudobulbar) lleva a desnutrición y patología respiratoria a repetición. Los trastornos de la motilidad intestinal sumados a un mal hábito alimentario contribuyen a constipación crónica. El reflujo gastroesofágico se asocia a trastornos dentales con defectos del esmalte, enfermedades gingivales, y caries.
La falta de un adecuado manejo postural y de la espasticidad lleva a posiciones viciosas, torsiones óseas y contracturas, lo que determina otras patologías como subluxación y luxación de caderas, contracturas dolorosas, deformidades osteoarticulares y escoliosis. La dificultad de aseo en zonas deformadas o de acceso limitado por las contracturas genera alteraciones de la piel e infecciones. De la interrelación de estas complicaciones surgen las medidas preventivas y terapéuticas: el uso de fármacos antiespásticos locales y sistémicos, manejo kinésico adecuado, órtesis, cirugías ortopédicas oportunas, permite que estas complicaciones puedan evitarse y/o manejarse oportuna y adecuadamente. (21).
El dolor es causa de irritabilidad y llanto persistente, difícil de objetivar y precisar causa por la limitada capacidad de comunicación. Como causas de dolor deben considerarse entre otras: hipoalimentación, caries dentales, distensión abdominal, constipación, infección urinaria, esogagitis por reflujo, hernia hiatal y contracturas.
Alternativas terapéuticas en PC
El tratamiento en las personas con parálisis cerebral tiene como objetivo lograr el máximo nivel de independencia o autonomía, lo que implica no solo el tratamiento motor sino muy importantemente el de los déficit asociados y las complicaciones. Hay estrategias preventivas, algunas resolutivas y muchas que permiten compensar o minimizar el déficit o trastorno que interfiere en la adquisición o desarrollo de funciones necesarias para la vida diaria.
Los tratamientos en PC han sido dirigidos a optimizar función, a tratar los efectos de la lesión de la primera neurona motora: espasticidad, distonía y otros movimientos involuntarios; a manejar los trastornos asociados (epilepsia, déficits sensoriales, etc.)y a tratar las complicaciones neurológicas y músculo esqueléticas a mediano y largo plazo.
Las alternativas terapéuticas disponibles en PC incluyen las intervenciones dirigidas al tratamiento de alteraciones del tono y la postura con fármacos, ejercicios, técnicas de estimulación y relajación y fisioterapia; a los trastornos asociados como la epilepsia, defectos sensoriales, y los déficits cognitivos con fármacos y estimulación cognitiva, entre otros; y a las complicaciones (contracturas musculares, deformidades, luxaciones, desnutrición con fármacos, procedimientos y cirugías). Los tratamientos disponibles, especialmente a nivel del trastorno motor permiten optimizar el desarrollo funcional y controlar las deformidades músculo esqueléticas que conducen a un deterioro agregado de la función motora en el tiempo.
Todas las intervenciones deben estar a cargo de equipo de múltiples especialistas: neurólogo, pediatra, ortopedista, fisiatra, psiquiatra, neurocirujano, kinesiólogo, fonoaudiólogo, terapeuta ocupacional, psicólogo, psicopedagogo, mejoran la calidad de vida de los pacientes con PC pero no son curativos, manteniendo un estado de discapacidad variable dependiendo de la severidad del compromiso.(22).
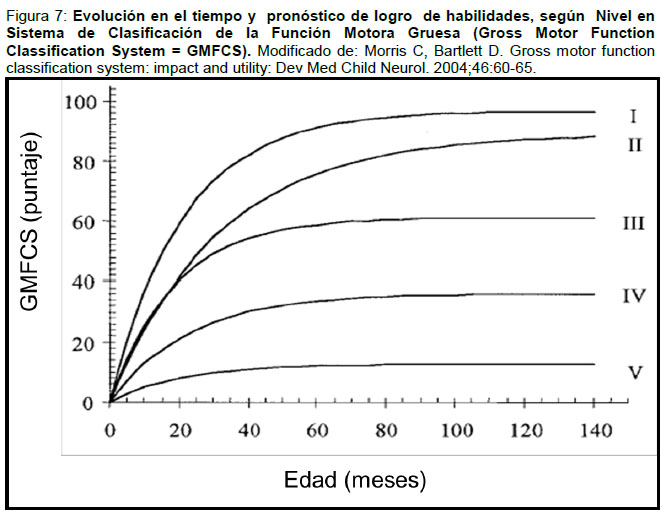
Es posible predecir hasta cierto punto, el nivel funcional que los pacientes alcanzarán según el compromiso motor. Esto se ha estudiado con el índice de función motora gruesa (GMFM) y se ha establecido a partir de éste un sistema de clasificación funcional (GMFCS) que determina una curva de desarrollo funcional de los niños con PC de acuerdo a su nivel de compromiso y su edad.(23) (Tabla 2 y Figura 7)
Líneas generales de tratamiento incluyen:
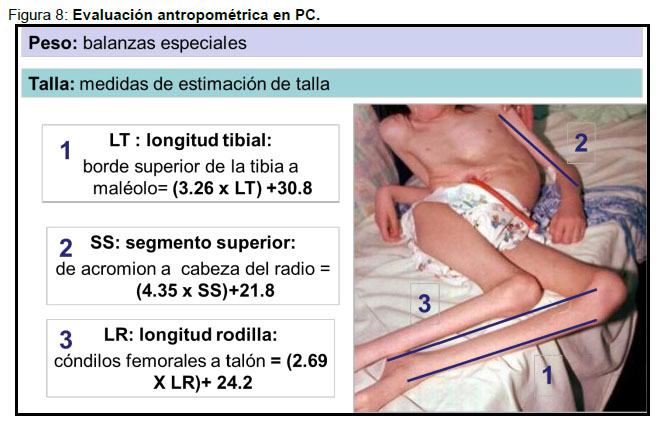
- Vigilar desarrollo y crecimiento pondoestatural adecuado, preocupándose del aporte nutricional, vitamínico, vacunas, acceso a beneficios como asignación de alimentos complementarios, doble asignación familiar etc. El manejo nutricional en PC tiene por objetivomantener la eutrofia y evitar estados carenciales (déficits selectivos vitamínicos o de micronutrientes). La evaluación pondoestatural en un niño con PC requiere: pesa adecuada, cálculo de talla (LT) medición de segmentos, cálculo de ingesta calórica y suplementación de vitaminas y oligoelementos: vitaminas D, C, A, B, ácido fólico, calcio. Es necesario considerar que una ingesta inadecuada puede producirse en todo niño con dependencia en las actividades de buscar e incorporar el alimento, derivado de las dificultades de comunicación, problemas de conducta o disfunción motora. Debe tenerse en cuenta además que morbilidades intercurrentes pueden generar exceso de pérdidas como en: infecciones a repetición, vómitos, y trastornos del movimiento con aumento de la actividad muscular sostenida (hipertonía, distonía). La estimación nutricional y cálculo de requerimientos nutricionales se muestra en Figura 8 y 9.
- Detección y tratamiento de infecciones, especialmente respiratorias.En niños con PC la función respiratoria se encuentra frecuentemente alterada y las enfermedades respiratorias son una causa frecuente de morbilidad. Por esto deben implementarse precozmente técnicas que permitan la mejor movilización de secreciones y óptima función ventilatoria. Se recomienda entrenar a los padres en técnicas de kinesiterapia respiratoria, de asistencia mecánica de la tos, vigilando su eficacia con seguimiento kinésico periódico; preverla aparición de insuficiencia respiratoria, buscando manifestaciones de cefalea matinal, fatigabilidad diurna, y/o anormalidades en el sueño; y el uso de ventilación asistida no invasiva en episodios respiratorios intercurrentes, con hiperinsuflación controlada de manera de evitar atelectasias.
- Detección de trastornos de la deglución y tratamiento precoz incluida indicación precoz de gastrostomía. Se recomienda considerar gastrostomía siempre con cirugía anti-reflujo en situaciones de ingesta insuficiente para asegurar crecimiento adecuado, y requerimiento de sonda nasogástrica por más de 2 meses, neumonías aspirativas recurrentes, tiempos de alimentación excesivamente largos, y/o rechazo alimentario.
- Manejo de la osteopenia: en la mayoría de los casos es de origen multifactorial, relacionada a la falta de movilización, baja ingesta de minerales, reducida absorción de vitamina D y/o alteración del metabolismo de vitamina D por fármacos antiepilépticos. Afecta mayormente a niños que no logran la marcha y que no mantienen bipedestación asistida en forma diaria. La osteopenia puede ser asintomática o manifestarse como fracturas atraumáticas. Las medidas preventivas de la osteopenia incluyen asegurar un aporte suficiente de vitamina D y calcio y la descarga diaria de peso mediante aparatos de bipedestación en niños no ambulantes. El tratamiento incluye suplementación con vitamina D, calcio y eventualmente bifosfonatos.
- Manejo del dolor: dolores crónicos y agudos se describen asociados a escaso movimiento, retracciones, deformidades articulares, osteoporosis, fracturas asociadas a traslados o movilización en hueso patológico. En el paciente con dificultades para comunicarse puede ser difícil su detección e identificación del origen o zona dolorosa. Se recomienda en estos casos: alto grado de sospecha, uso de escalas visuales de dolor, protocolos antiálgicos, con uso preventivo de analgésicos previo a actividades potencialmente dolorosas como las elongaciones de la terapia física, lo que mejora la cooperación del paciente.
- Manejo de la epilepsia: con el objetivo de lograr el mejor control de crisis, con la menor repercusión posible en el estado de vigilancia y efectos adversos en el paciente.
- Manejo ortopédico: El objetivo es limitar las retracciones articulares y escoliosis. En pacientes con pronóstico de marcha es clave mantener las extremidades inferiores alineadas compatibles con ella. En pacientes sin deambulación posible el objetivo es preservar la alineación de pies, pelvis y columna, evitando las complicaciones ortopédicas más frecuentes de pies (deformidad en equino), columna (escolisis) y pelvis: displasia, subluxación y luxación, causada por la hipertonía en músculos iliopsoas y aductores de muslos llevando a coxa valga con o sin anteversión femoral. Medidas de prevención incluyen disminuir el tono de los músculos más afectados: flexores y adductores de cadera en el caso de la pelvis y tríceps surales para prevenir equino, fármacos antiespásticos, neurotomías, y toxina botulínica.Vigilar estado dental con control odontológico preventivo y terapéutico periódico.
- Detección y manejo de las déficits asociados.
- Integración a educación y capacitación laboral de acuerdo a grado de discapacidad.
- Apoyo psicológico y/o psiquiátrico al niño y a la familia.
Tratamiento de las alteraciones del tono y la postura:
- Tratamiento de la espasticidad: El tratamiento farmacológico de la espasticidad comprende el uso de antiespásticos sistémicos, habitualmente agonistas GABA como las benzodiacepinas (diazepam, lorazepam, baclofeno) como también el uso de fármacos de administración local como la toxina botulínica. La inyección de esta toxina en músculos que presentan aumento de tono posibilita un mejor manejo de retracciones y permite también evaluar el resultado de ulteriores tenotomías en cuanto a funcionalidad. (24, 25).
- Tratamiento de los movimientos involuntarios: incluye un amplio arsenal de fármacos que se usan con resultados variables en el tratamiento de los diferentes movimientos anormales.(Revisado en 26)
- Uso de órtesis y otros aditamentos: las órtesis tobillo pie (OTP) son útiles en la prevención y tratamiento del equino en PC, especialmente si se usan en conjunto con férulas extensoras de rodilla que evitan retracción de isquiotibiales. La indicación de cojín abductor o aditamento separador de muslos permite evitar progresión de retracción de músculos adductores. Para implementar uso regular de órtesis se requiere que los padres hayan entendido los objetivos del uso de la órtesis y la revisión periódica de su indicación, tolerancia y adherencia. Las órtesis deben cumplir su objetivo, ser confortables y no producir lesiones, al igual que el uso de corsé que tiene por objetivo: limitar la progresión de la escoliosis y asegurar una sedestación estable y confortable.
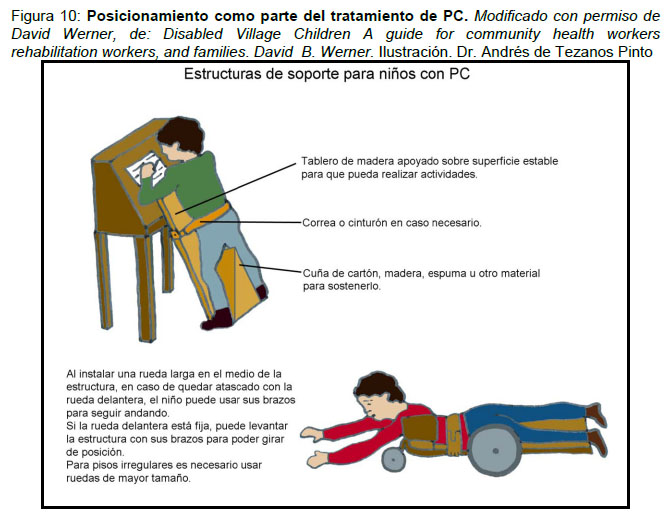
- Posicionamientos: Posicionamiento adecuado mantenido (varias horas al día) ayuda a mantener rangos articulares y a utilizar la gravedad en beneficio del niño. La clave es mantener las extremidades inferiores compatibles ortopédicamente con la bipedestación autónoma o asistida, y las grandes articulaciones (ej, caderas) en posición que permita disminuir el riesgo de luxaciones. Las alternativas de posicionamientos son intervenciones de bajo costo, y permiten optimizar todas las intervenciones basadas en las otras alternativas terapéuticas. Requieren de padres entrenados y terapeutas motivados en generar aparatos adecuados a cada niño con materiales accesibles para cualquier familia (Figura 10).
- Cirugía ortopédica: Procedimientos quirúrgicos ortopédicos deben considerarse con precaución por cuanto implican intervenciones definitivas.
- Manejo neuroquirúrgico: Procedimientos como rizotomía dorsal, bloqueos nerviosos, instalación de bombas de infusión para administración intratecal de fármacos antiespásticos, como el baclofén deben ser evaluados en cada caso.
- Terapia Física: Requiere definir objetivos concretos, medibles a corto mediano y largo plazo. Los objetivos pueden ser: aumentar las capacidades funcionales; prolongar o mantener la independencia para el funcionamiento y la movilidad; impedir las deformidades físicas y lograr la mejor integración en la sociedad, con buena calidad de vida. Existen múltiples modalidades o técnicas kinésicas utilizadas en el tratamiento del trastorno motor en Parálisis Cerebral, siendo las de Vojta y Bobath algunas de las más comúnmente usadas. Al menos 2 meta análisis que evalúan las intervenciones terapéuticas motoras en niños con o en riesgo de PC concluyen que no hay diferencias significativas entre diferentes intervenciones terapéuticas (27),lo que significa que se requieren más estudios bien diseñados que permitan definir si existen diferencias entre las distintos tipos de terapia física.
En síntesis el manejo pediátrico y neurológico en Parálisis Cerebral debe considerar:
- El tratamiento en PC es más que el manejo del problema motor.
- Requiere el trabajo de un equipo especializado y coordinado en la definición de objetivos, evaluación periódica y revisión de la metodología de evaluación.
- Seguimiento neurológico periódico a fin de prevenir, detectar y tratar precozmente complicaciones y trastornos asociados. Ej.: epilepsia, déficits sensoriales, etc.
- Fundamental es entrenar a los padres en estrategias e intervenciones que sea posible mantener en el tiempo para una neurorrehabilitación a largo plazo.
- Pediatra y neurólogo deben asumir la supervisión de:
- Cuidado pediátrico integral: desarrollo y crecimiento adecuado, vacunaciones al día, prevención de accidentes, vigilar estado dental y control odontológico periódico etc.
- Detección y tratamiento de infecciones, especialmente respiratorias.
- Detección y tratamiento precoz de trastornos de la deglución
- Guiar a la familia en acceso a beneficios (inscripción en el Servicio Nacional de la Discapacidad, SENADIS (28) doble asignación familiar etc).
- Apoyo psicológico y/o psiquiátrico al niño y a la familia: considerar costos económicos y emocionales que pueden llevar a empobrecimiento gradual y aislamiento social.
- Integración a educación y capacitación laboral: preparación para trabajos en ambientes protegidos.
Todo ello en el marco de los principios éticos fundamentales de beneficencia, no maleficencia, respeto por autonomía y justicia, esto es: proporcionar a todos los niños los cuidados necesarios en mismo estándar de calidad y cantidad (29).
Tablas y figuras


Referencias
- Bax MCO. Terminology and classification of cerebral palsy. Dev Med Child Neurol 1964;6:295-
- Badawi N, Watson L, Petterson B, Blair E, Slee J, Haan E, Stanley F. What constitutes cerebral palsy? Dev Med Child Neurol 1998;40:520-527.
- Shapiro BK. Cerebral palsy: a reconceptualization of the spectrum. JPediatr 2004;145:S3-S7.
- Boyd RN, Morris ME, Graham HK. Management of upper limb dysfunction in children with cerebral palsy: a systematic review. Eur J Neurol . 2001;8(suppl 5):150-166.
- Winter S, Autry A, Boyle C, Yeargin-Allsopp M. Trends in the prevalence of cerebral palsy in a population-based study. Pediatrics. 2002;110:1220-1225.
- Alberman E. Describing the cerebral palsies: methods of classifying and counting. In: Stanley F, Alberman E, eds. The epidemiology of the cerebral palsies. Philadelphia: JB Lippincott; 1984. p. 27-31.
- Hagberg B, Hagberg G, Beckung E, et al. Changing panorama of cerebral palsy in Sweden. VIII. Prevalence and origin in the birth year period 1991–94. Acta Paediatr 2001;90:271–277.
- Nelson KB, Ellenberg JH. Antecedents of cerebral palsy, I: univariate analysis of risks. Am J Dis Child 1985;139:1031-8.
- Nelson KB, Ellenberg JH. Antecedents of cerebral palsy: multivariate analysis of risk. N Engl J Med 1986;315:81-6.
- Harum KH,Hoon AHJr, Casella JF.Factor V Leiden: a risk factor for cerebral palsy. Dev Med Child Neurol 1999;41:781-5.
- Willoughby REJr, Nelson KB.Chorioamnionitis and brain injury.Clin Perinatol 2002;29:603-21
- Blickstein I , Keith LG.Outcome of triplets and high-order multiple pregnancies.Curr Opin Obstet Gynecol 2003;15:113-7.
- Hermansen MC. Perinatal Causes of Cerebral Palsy. Clinics in perinatology 2006;3 :xv-xvi DOI: 10.1016/j.clp.2006.03.015)
- Sanger TD, Delgado MR, Gaebler-Spira D, Hallett M, Mink JW, and the Task Force on Childhood Motor Disorders. Classification and definition of disorders causing hypertonia in childhood. Pediatrics. 2003;111:e89-e97.
- Delgado MR, Albright AL. Movement disorders in children: definitions, classifications, and grading systems. J Child Neurol. 2003;18(suppl 1):S1-S8.
- World Health Organization. International classification of functioning, disability, and health (ICF). Geneva: World Health Organization; 2001.
- Morris C, Bartlett D. Gross motor function classification system: impact and utility: Dev Med Child Neurol. 2004;46:60-65.
- Ashwal, S.; Russman, B.S.; Blasco, P.A.; Miller, G.; Sandler, A.; Shevell M, CM, FRCP; Stevenson R. Practice Parameter: Diagnostic assessment of the child with cerebral palsy. Report of the Quality Standards Subcommittee of the American Academy of Neurology and the Practice Committee of the Child Neurology Society. Neurology 2004;62:851–863.
- David Werner. Disabled Village Children A guide for community health workers rehabilitation workers, and families. Edición electrónica: Cap. 9 Cerebral palsy http://www.dinf.ne.jp/doc/english/global/david/dwe002/dwe00211.html#part1chap9
- Shapiro BK, Palmer FB, Capute AJ. Cerebral palsy: history and state of the art. In: Gottlieb M, Williams J, eds. Textbook of developmental pediatrics. New York: Plenum; 1987. p. 11-26.
- Tilton AH, Maria BL. Consensus statement on pharmacotherapy for spasticity. J Child Neurol. 2001;16:66-67.
- Gracies J-M, Elovic E, McGuire J, Simpson D. Traditional pharmacological treatments for spasticity. Part I: local treatments. Muscle Nerve. 1997a;20(suppl 6):S61-S91.
- Morris C, Bartlett D. Gross motor function classification system: impact and utility: Dev Med Child Neurol. 2004;46:60-65.
- Tilton AH. Approach to the rehabilitation of spasticity and neuromuscular disorders in children. Neurol Clin. 2003;21:853-881.
- Gracies J-M, Elovic E, McGuire J, Simpson D. Traditional pharmacological treatments for spasticity. Part II: general and regional treatments. Muscle Nerve. 1997b;20(suppl 6):S92-S120.
- Sanger T. Mink J. Movement Disorders. En: Swaiman K, Ashwal S, Ferreiro D, Schor N.(eds) Swaiman´s Pediatric Neurology. Principles and Practice. 5 ed. Elsevier 2012;965-998.
- Siebes R. ; Wijnroks L., Vermeer A. Qualitative analysis of therapeutic motor intervention programmes for children with cerebral palsy: an update. Dev Med Child Neurol 2002, 44: 593–603.
- http://www.senadis.gob.cl/
- Varela X, Kleinsteuber K, Avaria M:A_:Parálisis Cerebral En: David P., Förster J., Devilat M. Neurologia Pediatrica.. Editorial Mediterráneo 2012 Santiago-Chile. 1° Edición. Capítulo 53 páginas 407-414 ISBN 9562203417
|

