Introducción
El trauma es la principal causa de muerte en pediatría una vez cumplido el primer año de vida, permaneciendo como tal hasta los 45 años. En Chile, durante el año 2003 murieron 736 personas entre 1 y 19 años debido a Causas externas, lo que corresponde a más del 46% de las muertes para ese rango de edad (1).
En nuestro país, los accidentes de tránsito son responsables del 15% de todas las muertes entre 3 y 15 años. Luego, entre los 15-19 años adquieren relevancia las lesiones autoinflingidas, igualando en proporción a los accidentes de tránsito como causa de muerte (16% de todas las muerte, ambas) (1).
En cuanto a los motivos de hospitalización por trauma, el primer lugar es ocupado por el traumatismo encefalocraneano (TEC), que generó 4834 ingresos en el grupo de 0-14 años durante el año 2002, seguida de cerca por fractura de radio y cúbito (4782) y fractura de húmero (2145) (2).
La forma del cuerpo del niño y los mecanismos cerrados de lesión hacen que las lesiones multisistémicas sean más probables, por lo tanto se deben sospechar lesiones en todos los sistemas hasta demostrar lo contrario. Hay que considerar que los traumas cerrados más importantes son aquellos que comprometen el encéfalo, provocando alteraciones de ventilación como apnea, hipoventilación e hipoxia; esta situación es 5 veces más frecuente que la hipovolemia con hipotensión en niños (3). Esto justifica el énfasis que se debe dar al manejo de la vía aérea en el trauma pediátrico.
El rápido deterioro y desarrollo de complicaciones multisistémicas hace necesario el pronto traslado de estos pacientes a centros terciarios de salud, para lo cual es necesario la identificación de niños con trauma mayor en el escenario prehospitalario, adecuado manejo, destinación y uso de los recursos del servicio de urgencias.
Consideraciones especiales
En esta sección se hará mención de las principales diferencias anatómicas, fisiológicas y psicológicas entre el paciente pediátrico y el adulto, que tienen implicancia en el manejo del trauma pediátrico (3,4).
Anatómicas: Se mencionan en la Tabla 1. El menor tamaño corporal de los niños permite una amplia distribución de la energía favoreciendo los politraumatismos, además el mayor tamaño proporcional de la cabeza explica la mayor frecuencia de trauma cerrado con lesión cerebral en este tipo de pacientes.

El esqueleto no esta completamente calcificado, siendo más flexible. De este modo, se puede observar la presencia de importantes lesiones en pulmones, corazón o mediastino sin evidencias de fractura costal. Los cartílagos de crecimiento están en plena actividad, los cuales pueden lesionarse generando secuelas en el crecimiento de la extremidad.
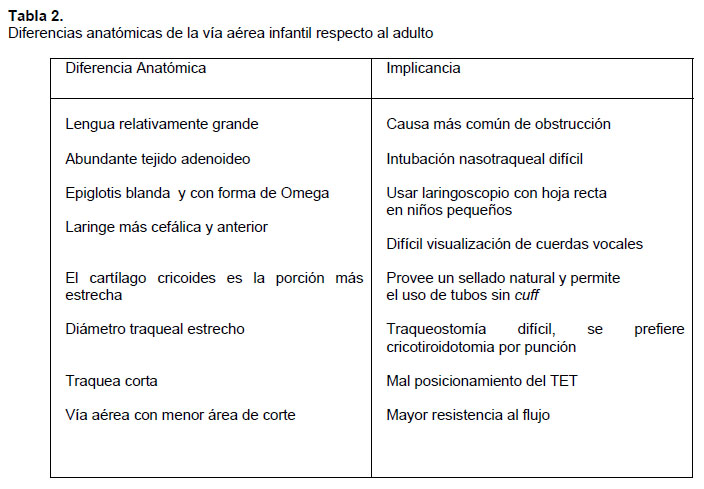
La vía respiratoria presenta características especiales que influyen en el momento de asegurarla. Estas son descritas en la tabla 2.
Fisiológicas: La mayor superficie corporal en proporción al peso favorece la pérdida de calor por evaporación, siendo necesario aumentar los aportes de agua libre, metales traza y minerales. Además, los requerimientos calóricos son proporcionalmente mayores en el niño lesionado que en el adulto.
Los niños presentan una reserva fisiológica elevada, por lo que a pesar de grandes pérdidas de sangre, los signos vitales permanecerán dentro de rango normal un mayor tiempo. La taquicardia y la mala perfusión cutánea son las únicas manifestaciones que permiten reconocer la hipovolemia de manera precoz e iniciar reanimación con cristaloides.
Psicológicas: es frecuente observar comportamientos regresivos frente al estrés y el dolor cuando todavía no desarrollan habilidades suficientes para enfrentar estas situaciones, por lo que se debe tranquilizar al niño y entablar una buena relación medico-paciente. Hay que destacar que un 25% de los niños que sufren accidentes de tránsito presentarán síntomas de estrés postraumático al alta (5).
Efectos a largo plazo . Incluso lesiones leves pueden asociarse a discapacidad prolongada, la que puede manifestarse a nivel de la función cerebral, ajuste psicológico o alteraciones de otros órganos. Un 60% de niños con trauma grave multisitémico presentan cambios residuales de personalidad al año del alta y un 50% presenta algún deterioro cognitivo o físico (3).
Las lesiones en cartílagos de crecimiento pueden provocar serias repercusiones: asimetrías en el largo del fémur pueden generan alteraciones de la marcha y daño en los centros de crecimiento vertebrales con secuelas como deformidades de la columna vertebral.
Por otra parte, daños en órganos sólidos también pueden generan secuelas importantes. Una esplenectomía realizada para tratar una ruptura masiva del bazo, predispone a infecciones sistémicas bacteriana posteriormente.
Fase prehospitalaria
Consiste en sospechar un traumatismo grave, realización del ABCDE del trauma prehospitalario, triage cuando corresponda y traslado (6).
La decisión de inmovilización de un paciente se basa en la historia y el examen físico. Entre los mecanismos de lesión que presentan alto riesgo de injuria cervical se encuentran: mecanismos de alta energía, lesiones por buceo o zambullidas y lesiones por mecanismo de aceleración – desaceleración. La presencia de alteración de conciencia, incapacidad para cooperar o verbalizar, dolor en la línea media posterior cervical, disminución del rango de movimiento, déficit neurológico o trauma multisistémico son muy sugerentes de lesión cervical, a pesar que el paciente sea capaz de caminar (7).
El traslado debe realizarse al sitio más cercano y apropiado; si es posible, especializado en trauma. Siempre se debe establecer comunicación con el lugar de derivación previo al arribo del paciente, notificando al equipo de trauma. Se puede anticipar la necesidad de personal especializado (cirujano infantil, neurocirujano, intensivista) frente a situaciones de (8):
- Alteración de vía aérea, respiración o circulación
- Nivel de conciencia alterado
- Sospecha de lesión espinal
- Quemaduras extensas
- Trauma penetrante.
- Accidentes de alta energía (caídas de gran altura, colisiones vehiculares con muertos).
Fase hospitalaria
Revisión primaria
El objetivo de la revisión primaria es determinar rápidamente si existe alguna condición de riesgo vital que requiera tratamiento inmediato, reanimar y controlar funciones vitales; estas acciones se realizan simultáneamente. Los signos vitales se deben repetir cada 5 minutos durante la revisión primaria, y después cada 15 minutos, hasta que el paciente se encuentre estable. El orden de esta evaluación corresponde al ABCDE de la atención del trauma (3):
A: Airway. Mantenimiento de la vía aérea y control de la columna cervical.
B: Breathing . Respiración y Ventilación.
C: Circulation. Circulación con control de la hemorragia
D: Disability. Déficit Neurológico.
E: Exposure. Exposición / Control ambiental
A lo anterior puede agregarse (4):
F: Family Familia
A. – Vía aérea :
El objetivo de esta etapa es mantener una vía aérea permeable protegiendo la columna cervical.
El primer paso es evaluar si la vía aérea está permeable y protegida. Si hay fonación audible o ruidos respiratorios la vía esta permeable, aunque una respiración ruidosa sugiere obstrucción parcial. La presencia de reflejo faríngeo y capacidad de tragar saliva nos indican una adecuada protección de la vía aérea. Se debe descartar la presencia de cuerpos extraños, fracturas faciales, mandibulares, de la traquea o laringe que puedan generar obstrucción.
El manejo, llevado a cabo simultáneamente, debe considerar (9):
Posicionamiento : La permeabilidad de la vía aérea se puede conseguir mediante las maniobras de elevación del mentón y levantamiento de la mandíbula asociado a inmovilización espinal bimanual en línea.
Monitorización cardiorrespiratoria y oximetría de pulso. Capnografía cuando está disponible, ya que en pacientes con depresión respiratoria, se puede detectar un aumento del dióxido de carbono de final de espiración (End Tidal CO2, ETCO2) antes que la hipoxemia sea evidente.
Oxígeno : Eliminar secreciones de la orofaringe previamente.
Descompresión gástrica : niños que han sido ventilados rápidamente o que hayan utilizado dispositivos de ventilación con presión positiva pueden desarrollar distensión gástrica dificultando la excursión diafragmática (10). De este modo, la utilización de sonda orogástrica o nasogátrica puede favocer la ventilación.
Los métodos mecánicos de mantención de la vía aérea son: cánula orofaríngea, intubación orotraqueal y cricotiroidotomía por punción (3). La cánula orofaríngea debe usarse únicamente cuando el niño está inconciente, de lo contrario puede desencadenar el vómito. La intubación orotraqueal se prefiere a la nasotraqueal; esta última no debe realizarse en menores de 9 años por las dificultades que genera el ángulo agudo de la faringe posterior, el potencial empeoramiento de sangrado en la cavidad oral y el incremento de la presión intracraneana. Las indicaciones de intubación orotraqueal se encuantran en la Tabla 3, sin embargo, debe tenerse en cuenta que, en la fase, prehospitalaria la ventilación con máscara y bolsa es efectiva y más segura que la intubación (11).

En niños menores de 8 años, sin disminución de la distensibilidad pulmonar, sin resistencia elevada de la vía aérea y sin un gran escape de aire a través de la glotis, se recomienda utilizar tubo sin manguito inflable
(uncuffed endotracheal tube) (12). Para determinar el diámetro interno adecuado, existen las siguientes fórmulas utilizadas en niños entre 1 y 10 años (4):
Tubo endotraqueal sin cuff ( mm) = (edad en años + 16)/4
Tubo endotraqueal con cuff (mm) = (edad en años + 12)/4
La mayoría de los centros de atención del trauma utilizan un protocolo para la intubación de urgencias, llamado Secuencia Rápida de Intubación ( Rapid sequence intubation, RSI) , el cual describe un proceso secuencial de preparación, sedación y parálisis que facilita la intubación de emergencia. Este protocolo se resume en los siguientes pasos (3, 13, 14):
a. Preoxigenación: Comenzar de inmediato cuando la decisión de intubar es considerada. Administrar oxígeno en la más alta concentración posible.
b. Preparación: Consiste en identificar condiciones que puedan afectar la elección de medicamentos y que sean predictores de intubación difícil, armar equipo y chequear, desarrollar plan de contingencia en caso de que la intubación fracase.
c. Pretratamiento: La manipulación de la vía aérea con el laringoscopio puede desencadenar incremento o disminución de la frecuencia cardíaca, incremento de la presión intracraneana, y elevación de la presión arterial y de la resistencia de la vía aérea. Estas respuestas pueden ser atenuadas mediante la utilización de atropina en dosis de 0.02 mg/kg/iv (máx 0.5 mg; min 0.1 mg) administrada 1 ó 2 minutos antes de la intubación; o lidocaína, si la presión intracraneana está elevada, en dosis de 1 a 1.5 mg/kg/iv. También se pueden utilizar opiodes y relajantes musculares desfasciculantes.
d. Sedación: Los fármacos a utilizar dependen de la presencia de inestabilidad cardiovascular, alteraciones neurológicas (convulsiones, hipertensión endocraneana) o broncoespasmo:
- Etomidato: Seguro en pacientes hemodinámicamente inestables, neuroprotector, produce corticosupresión adrenal transitoria. No usar en caso de convulsiones focales. Dosis de 0.03
g/kg/IV
- Tiopental: Neuroprotector. No usar si hay inestabilidad hemodinámica. Dosis de 3 a 5 mg/kg/IV
- Ketamina: Seguro en pacientes hemodinámicamente inestables si no presentan depleción catecolaminérgica. Usar si hay broncoespasmo. No usar en caso de hipertensión endocraneana. Dosis de 1 a 2 mg/kg IV
- Midazolam: Requiere mayor tiempo para producir efecto e induce inconciencia de manera inconsistente. Puede causar inestabilidad en dosis requeridas para sedación. Dosis: 0.3 mg/kg IV.
Después de la sedación se mantiene presión sobre la región cricoídea para evitar aspiración de contenido gástrico
e. Parálisis: Los agentes paralíticos generan una relajación muscular completa, lo que facilita la intubación. El fármaco ideal es aquel que cause parálisis de corta duración, como la succinilcolina.
- Succinilcolina: contraindicado en caso de miopatía crónica o denervación neuromuscular, 48-72 hrs después de quemaduras, lesiones por aplastamiento, hipertermia maligna, o hiperkalemia preexistente. Dosis: si < 10 kg usar 2 mg/kg; si >10kg usar 1 mg/kg.
- Rocuronio: Usado cuando existe contraindicación a succinilcolina. Dosis de1 mg/kg.
f. Protección y posicionamiento: Posicionar la cabeza con el conducto auditivo externo anterior al hombro con la nariz y boca apuntando al techo. Aplicar presión sobre cartílago cricoides una vez que el niño esté inconciente. Mantener presión hasta que se verifique posición del tubo endotraqueal (TET).
g. Posicionamiento con colocación: La parálisis ocurre entre 30-60 segundos luego de la administración de los paralíticos. Cuando se confirma una adecuada relajación, se procede con la laringoscopía. Luego , se debe confirmar la ubicación del tubo con auscultación y ETCO2.
h. Manejo Post-intubación: Radiografía de tórax para evaluar ubicación del TET, aportar sedación continua, analgesia y paralíticos.
Finalmente, cuando el acceso y control de la vía aérea no se pueden conseguir mediante dispositivo de mascara y bolsa o intubación endotraqueal, el método de elección es la cricotiroidotomía por punción, que consiste en la insuflación de aire a presión a través de una aguja introducida en la membrana cricotiroidea. Sin embargo, esta técnica no permite una buena oxigenación y puede ocurrir retención de CO2. Por otra parte, la cricotiroidotomía quirúrgica puede realizarse de manera segura en mayores de 12 años (3).
B. – Respiración y Ventilación:
Evaluar frecuencia respiratoria y expansión torácica. Una frecuencia demasiado rápida o lenta para la edad indica una insuficiencia respiratoria inminente, por lo que el paciente debe recibir ventilación asistida. Los dispositivos de bolsa y máscara (Ambú) cuentan con válvula de seguridad, sin embargo se debe tener la precaución de aportar sólo el volumen necesario para elevar el tórax, de lo contrario se favorece la distensión gástrica produciendo mayor dificultad respiratoria.
Se debe considerar la presencia de neumotórax o hemotórax en pacientes con fracturas de costillas, disminución de murmullo pulmonar, yugulares distendidas o desviación traqueal. Estas lesiones deben ser tratadas rápidamente mediante aguja o tubo de toracostomía. El sitio de inserción es el 5° espacio intercostal (igual que adultos), en la línea axilar anterior, pasando sobre la costilla, hacia arriba y atrás (3).
C. – Circulación:
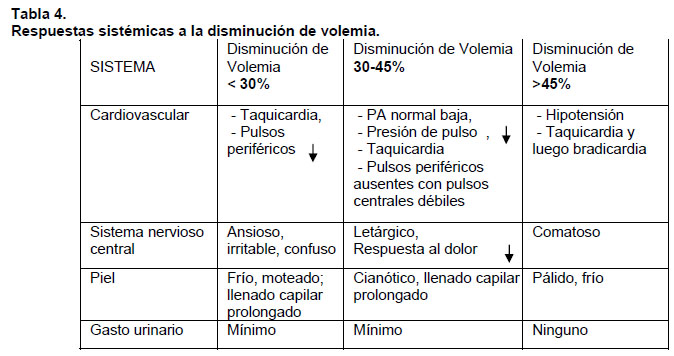
Evaluación. Comprende la valoración del pulso, color de la piel y tiempo de llene capilar. Una presión arterial sistólica (PAS) normal no asegura una adecuada hemodinamia, debido a que los niños poseen una gran reserva fisiológica, siendo necesaria una perdida de más del 45% de la volemia para generar hipotensión. En consecuencia, la presencia de taquicardia, frialdad de extremidades, disminución del pulso periférico versus el central y mala perfusión cutánea, aún con presión mantenida, pueden ser las únicas manifestaciones de un shock hipovolémico con lo que se debe comenzar la reanimación con líquidos (15, 16).
La tabla 4 muestra la respuesta sistémica de acuerdo a la magnitud de la hipovolemia (6). En general, un pulso periférico palpable se correlaciona con una PAS mayor a 80 mm Hg, y un pulso central palpable lo hace con una PAS mayor a 50 -60 mm Hg. Las presiones más bajas consideradas normales para una determinada edad son las siguientes (12).
- 60 mm Hg en RN de término
- 70 mm Hg en Lactante Menor
- 70 mm Hg + (2 x edad) en niños de 1 a 10 años
- 90 mm Hg en niños > 10 años
El paciente debe recibir monitorización cardíaca, aporte de oxígeno y reevaluación constante de signos vitales junto con oximetría de pulso.
Accesos Venosos: Se deben instalar 2 vías venosas de grueso calibre de preferencia en extremidad superior. Los sitios disponibles para el acceso venoso se mencionan en la tabla 5 (17). Cuando se necesita acceso inmediato o no hay éxito en establecer una vía venosa luego de 5 minutos de intentos, se debe utilizar la vía intraósea. Los sitios son:

- Tibia proximal: 1cm abajo y medial a la tuberosidad tibial
- Tibial distal: por medial, 1 -2 cm proximal al maléolo medial.
- Tercio distal del fémur: en la línea media, 3 cm arriba del cóndilo medial.
Una vez instalado los catéteres se debe obtener muestras de sangre para determinar grupo sanguíneo, Rh y exámenes de laboratorio (hematocrito, gases, pruebas hepáticas, amilasas, etc.)
Reanimación con líquidos y reeplazo de sangre: La volemia de un niño es aproximadamente 80 ml/kg. Para reponer volumen se utilizan soluciones cristaloides isotónicas con la precaución que el líquido esté caliente (37- 39°C) para no favorecer la hipotermia. Se administran bolos de 20 ml/kg de solución Ringer Lactato en 10 minutos, considerando que sólo el 25% del volumen administrado permanecerá en el espacio intravascular. Si ya hemos completado 40ml/kg y un tercer bolo es requerido para revertir los signos de hipoperfusión, se debe considerar administrar un bolo de 10 ml/kg de concentrado de glóbulos rojos tipo específico o tipo O negativo (3). Sin embargo, si sospechamos que un sangrado oculto es la causa de un shock hemodinámico con insuficiencia cardíaca o pulmonar, debe administrarse cristaloides y concentrado de glóbulos rojos simultáneamente(4).
A diferencia del adulto, el shock cardiogenico es poco común en niños; sin embargo, ante la presencia de trauma torácico asociado a shock se debe considerar la posibilidad de contusión o ruptura del miocardio (18).
Las decisiones terapéuticas dependen de la respuesta del paciente a la reanimación con líquidos:
- Respuesta rápida a la administración inicial de fluidos: no requiere nuevos bolos.
- Respuesta transitoria: administrar un segundo o tercer bolo más glóbulos rojos. Posiblemente requiera cirugía.
- Respuesta mínima o sin respuesta: Intervención quirúrgica inmediata para controlar hemorragia exanguinante.
Resucitación Cardiopulmonar (RCP): Actualmente, se recomienda una proporción de masaje-ventilación de 30:2 cuando la RCP es realizada sólo por una persona, y 15:2 si es realizada por 2 personas (19). Esto se justifica porque al disminuir las interrupciones del masaje cardiaco, mejora la presión de perfusión coronaria, aumentando la probabilidad de retornar a circulación espontánea. Por otra parte, la utilización de altas dosis de epinefrina no es recomendada, excepto si es administrada por TET o en caso de sobredosis por Beta – Bloqueadores.
Monitorización: La normalización hemodinámica estará indicada por:
- Normalización de la frecuencia cardíaca
- Mejoría del nivel de conciencia
- Color de piel normal
- Aumento de temperatura de extremidades
- Aumento de la PAS
- Aumento de la presión de pulso
- Diuresis de 1 a 2 ml/Kg/hora
D. – Déficit Neurológico: Esta etapa consiste en una rápida evaluación neurológica con el fin de determinar el nivel de conciencia, tamaño y reacción pupilar, signos de lateralización y nivel de lesión medular. Para determinar el nivel de conciencia son útiles la Escala de Coma de Glasgow (GCS) y el Sistema AVPU (cuadro 1 y 2).


Los niños con alteración de conciencia secundaria a trauma craneoencefálico tienen un alto riesgo de compromiso de vía aérea y lesiones cerebrales secundarias, de aquí la importancia de la temprana intubación endotraqueal y ventilación con presión positiva (20).
Es muy importante descartar una hipoglicemia como causa de alteración de conciencia, ya que las reservas de glicógeno en el paciente pediátrico rápidamente se depletan, favoreciendo dicha condición (4).
E. – Exposición: Este paso comprende desvestir al paciente para descartar otras lesiones que permanezcan ocultas. Se debe tener presente que la hipotermia puede complicar la reanimación, por lo que se debe evitar la pérdida excesiva de calor. Se pueden utilizar lámparas de calor durante el examen, cubrir al paciente con mantas y calentar los fluidos endovenosos con este fin (21).
F. – Familia: Durante el manejo del niño traumatizado, los familiares deben ser informados rápidamente de lo que esta ocurriendo para disminuir de este modo la angustia. Se debe permitir la presencia de familiares durante la reanimación si ellos lo desean, y se debe encargar a un miembro del equipo del equipo de trauma que le explique los procedimientos que se van realizando (22).
Evaluación Secundaria
La evaluación secundaria empieza una vez que se ha reanimado al paciente y que sus signos vitales se estabilizan. Su propósito es identificar lesiones potencialmente fatales que no fueron identificadas durante la evaluación primaria. En la evaluación secundaria se realiza:
- Historia médica considerando los puntos claves de la mnemotécnica AMPLE (cuadro 3),
- Examen físico de pie a cabeza,
- Terapia antibiótica cuando hay indicación,
- Monitorización de signos vitales de manera continua.
- Se asegura una diuresis de 1 ml/kg/hora.
- Exámenes imagenológicos y de laboratorio pertinentes

Examen Físico:
- Cabeza: Evaluar tamaño y reactividad pupilar, fondo de ojo, palpación de cráneo. El paciente debe permanecer con collar cervical hasta que se descarte lesión cervical.
- Tórax: Inspeccionar buscando heridas y fracturas. Palpar observando dolor y crepitaciones. Auscultación buscando signos de ocupación pleural o alteraciones cardiacas.
- Abdomen: El examen físico abdominal no es útil si el paciente presenta una lesión encefálica o está en GCS <13(23)
- Tacto rectal: Evalúa tono del esfínter, posición de la próstata y sangre en deposiciones.
- Buscar: sangre en el meato uretral, hematoma perineal o abdominal bajo.
- Extremidades: buscar deformidades, heridas y evaluar perfusión.
Pruebas diagnósticas: Estás son indicadas de acuerdo a lo observado durante la evaluación secundaria, la edad del paciente y el mecanismo del trauma.
a) Laboratorio:
- Hemoglobina o hematocrito y grupo sanguíneo.
- Un urianálisis o dipstick urinario pueden revelar la presencia de hematuria, identificando lesiones renales o abdominales (24).
- Los adolescentes deben ser evaluados por posible uso de drogas o alcohol.
b) Radiología.
- Radiografía de tórax, lateral cervical, de pelvis y extremidades afectadas.
- Abdomen: La tomografía computada (TC) sin contraste es el método de elección frente a sospecha de lesión abdominal en paciente estable; la ecografía también es útil, pero menos sensible, debiendo confirmarse con TC posteriormente (25). El lavado peritoneal diagnóstico tiene una utilidad limitada puesto que las lesiones de vísceras sólidas frecuentemente se presentan sin fluido peritoneal, y por otra parte, la sola presencia de fluido no es necesariamente indicación de cirugía.
- Las indicaciones de TAC de cerebro se mencionan en el cuadro 4.

- Los niños menores de 2 años con lesiones por abuso requieren evaluación del esqueleto y radiografías de cráneo, tórax, abdomen y huesos largos (4).
Consideraciones finales: Los pacientes no deben permanecer más de 2 horas en la tabla espinal por el riesgo de escaras, esta se debe retirar apenas se hayan descartado lesiones torácicas o lumbares; a su vez, el collar cervical debe permanecer puesto hasta que la radiografía descarte lesiones (3). Sin embargo, si la clínica es muy sugerente de lesión, aún con radiografías normales, el paciente debe ser manejado como si estuviese lesionado.
El paciente debe ser continuamente reevaluado hasta que comience el tratamiento médico definitivo.
Referencias
- Instituto Nacional de Estadísticas (INE). Compendio Estadístico, Chile, 2005.
- Medina E, Kaempffer A. Consideraciones epidemiológicas sobre los traumatismos en Chile. Rev. Chilena de Cirugía 2007; 59 (3): 175-84.
- American college of surgeons. Advanced Trauma Life Support (ATLS) student course manual. 7th edition. Chicago: American College of Surgeons; 2004.
- Avarillo J, Cantor R. Pediatric Major Trauma: An Approach to Evaluation and Management. Emerg Med Clin N Am 25 (2007) 803–36.
- Schafer I, Barkmann C, Riedesser P, et al. Posttraumatic syndromes in children and adolescents after road traffic accidentsda prospective cohort study. Psychopathology 2006;39(4):159–64.
- Ministerio de Salud de Chile. Guía Clínica Politraumatizado. 2007
- Hoffman JR; Mower WR; Wolfson AB; Todd KH; Zucker MI. Validity of a set of clinical criteria to rule out injury to the cervical spine in patients with blunt trauma. National Emergency X-Radiography Utilization Study Group. N Engl J Med 2000 Jul 13;343(2):94-9
- Prehospital triage criteria. In: Advanced trauma life support, Alexander, RH, Procter, HJ (Eds), American College of Surgeons, Chicago 1993. p.319.
- Wang V. Airway management in children. In: UpToDate, Rose, BD (Ed), UpToDate, Waltham , MA , 2007.
- Berg MD; Idris AH; Berg RA. Severe ventilatory compromise due to gastric distention during pediatric cardiopulmonary resuscitation. Resuscitation 1998 Jan;36(1):71-3.
- Gausche M, Lewis RJ, Stratton SJ, et al. Effect of out-of-hospital pediatric endotracheal intubation on survival and neurological outcome: a controlled clinical trial. JAMA 2000;283:783–9.
- Part 12: Pediatric Advanced Life Support. Circulation 112: IV-167-187IV-; publicada en línea previo a impresión: http://dx.doi.org/doi:10.1161/CIRCULATIONAHA.105.166573
- Agrawal D. Rapid sequence intubation in children. In: UpToDate, Rose, BD (Ed), UpToDate, Waltham , MA , 2007.
- Gerardi MJ, Sacchett AD, Cantor RM et al: Rapid-sequence intubation of the pediatric paticnt. Annals of Emergency Medicine July 1996; 28: 55-74.
- Pediatric Advanced Life Support Provider Manual. Zaritsky , AL , et al (Eds), American Heart Association, Subcommittee on Pediatric Resuscitation, Dallas , 2002.
- Schwaitzberg SD ; Bergman KS ; Harris BH . A pediatric trauma model of continuous hemorrhage. J Pediatr Surg 1988 Jul;23(7):605-9.
- Kanter RK, Zimmerman JJ, Strauss RH, et al. Pediatric emergency intravenous access. Evaluation of a protocol. Am J Dis Child 1986;140:132–4.
- Furnival RA. Delayed diagnosis of injury in pediatric trauma. Pediatrics 1996;98:56–62.
- ECC Committee, Subcommittees and Task Forces of the American Heart Association. 2005 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation 2005 Dec 13; 112:Suppl:IV-1-IV-211.
- Chesnut RM; Marshall LF; Klauber MR; Blunt BA; Baldwin N; Eisenberg HM; Jane JA; Marmarou A; Foulkes MA. The role of secondary brain injury in determining outcome from severe head injury. J Trauma1993 Feb;34(2):216-22.
- Bernardo LM; Gardner MJ; Lucke J; Ford H. The effects of core and peripheral warming methods on temperature and physiologic variables in injured children. Pediatr Emerg Care 2001 Apr;17(2):138-42.
- Brown K, Bocock J. Update in pediatric emergecy resuscitation. Emerg Med Clin NorthAm 2002;20(1):1–26.
- Holmes JF, Sokolove PE , Brant WE, et al. Identification of children with intraabdominal injuries after blunt trauma. Ann Emerg Med 2002;39:500–9.
- Isaacman DJ; Scarfone RJ; Kost SI; Gochman RF; Davis HW; Bernardo LM; Nakayama DK. Utility of routine laboratory testing for detecting intra-abdominal injury in the pediatric trauma patient. Pediatrics 1993 Nov;92(5):691-4.
- Hampers L. Approach to the injured child. In: UpToDate, Rose, BD (Ed), UpToDate, Waltham , MA , 2007.
|

