Introducción
El bloqueo aurículoventricular (BAV) se denomina completo, cuando todas las ondas P fallan al momento de conducir hacia los ventrículos; descrito por primera vez en 1901 por Morquio y asociado a muerte súbita en infantes. (1) Es una enfermedad autoinmune que se desarrolla entre las 16 y 24 semanas de gestación con una incidencia de 1 en 17 000 nacidos vivos. (2) Esta alteración en la conducción cardiaca que necesariamente inicia a nivel uterino es importante diferenciarla de la bradicardia producto de un distress fetal. (3) (4) Una vez realizado el diagnóstico intrauterino está indicada la realización de ecocardiografía fetal para descartar patologías cardiacas asociadas como isomería izquierda o inversión ventricular, en cuyos casos la mortalidad es elevada. Sin embargo el bloqueo cardíaco también puede presentarse de forma aislada lo que mejora el pronóstico en este grupo con una supervivencia a largo plazo cercana al 90%. (4) El tratamiento consiste en el implante de un marcapasos permanente con indicación Clase I o IIb de acuerdo a las características clínicas acompañantes. (5)
Caso clínico
Preescolar de 2 años de edad, sexo masculino. Antecedentes prenatales: madre de 29 años, gestas previas 1, partos 1, hijos vivos 1, controles prenatales completos sin alteraciones, toma hierro y vitaminas desde el primer trimestre. Se realizó tres ecografías obstétricas que resultaron normales y un ecocardiograma prenatal de rutina a las 22 semanas de gestación que no reportó alteraciones.
Antecedentes natales: nace por parto eutócico a las 40 SG sin complicaciones, llanto inmediato, apgar 9/9, y alojamiento conjunto adecuado con medidas antropométricas dentro de parámetros de normalidad.
Antecedentes postnatales: esquema de vacunación y desarrollo psicomotor adecuado para la edad, estado nutricional eutrófico (peso 11 kg, talla 91 cm). No antecedentes de hospitalizaciones. Antecedente familiar ninguno de interés.
Preescolar asintomático es valorado por el servicio de cardiología pediátrica por encontrarse una frecuencia cardíaca de 40 latidos por minuto (lpm) en una valoración pediátrica de rutina. Al examen físico además de la bradicardia no hubo ningún otro hallazgo patológico.
Exámenes complementarios:
- Hemograma, coagulograma y química sanguínea dentro de rangos de normalidad.
- Radiografía de tórax (figura 1) normal
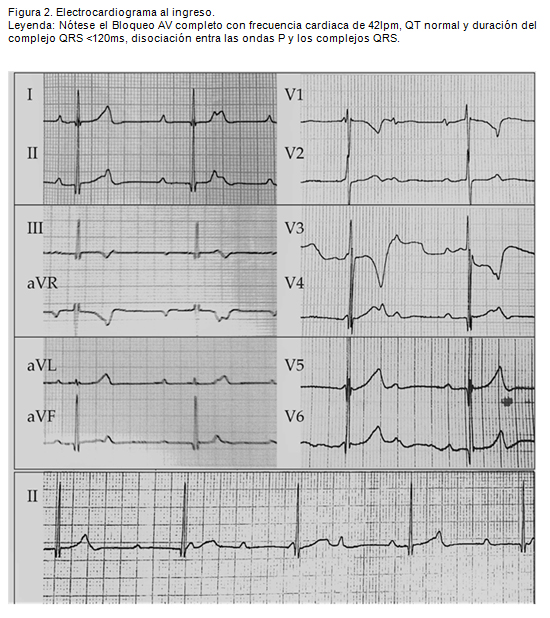
- Electrocardiograma (ECG) de 12 derivaciones (figura 2) con un BAV completo, con una frecuencia ventricular de 42 lpm, intervalo QTc mediante la fórmula de Bazett de 385ms y una duración del complejo QRS de 80 ms.
- Ecocardiograma sin alteraciones, con una fracción de eyección del ventrículo izquierdo (FEVI) del 76%, diámetros y volúmenes dentro de rangos de normalidad, aparatos valvulares competentes, no masas, contractibilidad global y segmentaria adecuada.
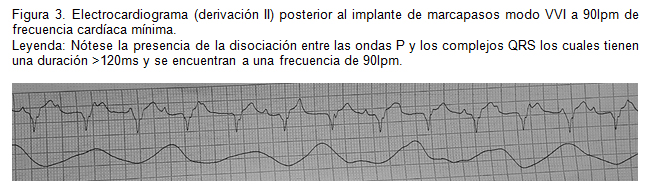
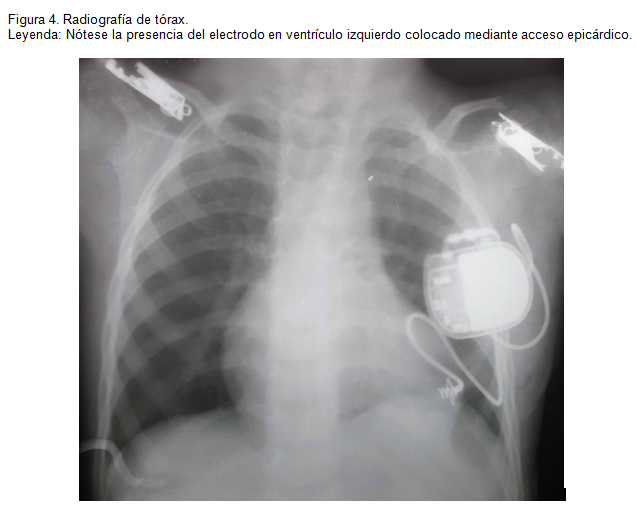
Se procedió a implantar marcapasos monocameral con colocación de electrodo epicárdico en ventrículo izquierdo, procedimiento sin complicaciones. Se programó el marcapasos en modo VVI (V: estimulación ventricular; V: sensado ventricular; I: respuesta inhibitoria ante el sensado ventricular positivo) a 90lpm, permaneció monitorizado por 24 horas sin presentar fallo del dispositivo ni complicaciones durante ese tiempo. Se complementa con un ECG (figura 3) donde se evidencia ritmo de marcapasos a 90lpm además se repitió la radiografía de tórax (figura 4) observando tanto el generador como los cables en correcta ubicación e íntegros; el paciente permaneció hospitalizado bajo monitorización continua por 24 horas y fue dado de alta sin complicaciones.
Comentarios
Si bien teóricamente la presencia de este bloqueo está presente desde la fase intrauterina no es infrecuente que el diagnóstico se realice en controles posteriores debido a la variabilidad de la progresión del mismo que puede presentarse en primeras instancias como bloqueo de primer o segundo grado y avanzar hasta el bloqueo completo en dependencia de la susceptibilidad inmunológica de cada individuo. (4)
La presentación clínica del BAV completo está relacionada con la frecuencia cardiaca ventricular, la respuesta cronotrópica al esfuerzo físico, así como a la respuesta hemodinámica del miocardio ante la bradicardia sostenida que puede expresarse como una cardiomiopatía dilatada en algunos casos. Aunque la mayoría de pacientes con BAV aislado se encuentran asintomáticos al momento del diagnóstico, también existe un grupo de pacientes quienes debutan con muerte súbita cardíaca (5) (6) y otros pueden presentar síntomas inespecíficos, como crecimiento deficiente, cansancio anormal, alteraciones del sueño o pesadillas frecuentes. (7)
El diagnóstico definitivo se realiza mediante el electrocardiograma en donde se observa una disociación auriculo-ventricular, es decir la onda P que refleja la actividad auricular y el complejo QRS que representa la actividad ventricular ocurren aisladamente sin la sincronía normal. Esta disociación produce una relación P-R variable asociada a un ritmo ventricular regular, debido a que la frecuencia auricular siempre es más rápida que la ventricular y a que el impulso auricular nunca es conducido hacia los ventrículos, tal como se observa en este caso (figura 1). (8) (9) Es importante analizar el ECG basal en busca de un intervalo QTc prolongado cuya asociación implica la necesidad de un implante de marcapasos permanente, en este caso el intervalo QTc fue normal (385ms). (5) (10)
El BAV completo congénito generalmente se localiza por encima del sistema His-Purkinje, que se expresa en el electrocardiograma con un QRS estrecho y una frecuencia cardíaca entre 40 y 60 lpm, lo que también se observó en este paciente (QRS 80ms con una FC de 42lpm). (8)
La conducta terapéutica frente a un BAV completo congénito se enfoca en la prevención de ataques de Adam-Stokes y de la aparición de insuficiencia cardíaca a cualquier edad, por lo que no se debe posponer innecesariamente la estimulación cardiaca con marcapasos cuando está indicada ya que aumenta el riesgo de presentar muerte súbita cardiaca. (5)
En pacientes sintomáticos, es decir con sincope, presíncope o incompetencia cronotrópica que limite la actividad física está recomendado el implante de marcapasos (Indicación Clase I Nivel de evidencia C). En asintomáticos la estimulación cardíaca permanente es recomendada ante la presencia de patologías de riesgo asociadas como son: disfunción ventricular, intervalo QTc prolongado, ectopia ventricular compleja, ritmo de escape QRS ancho, ritmo ventricular menor a 50 lpm y pausas ventriculares 3 veces mayores que el ritmo subyacente. (Indicación Clase I Nivel de evidencia C). En pacientes que no cumplen las características antes mencionadas el implante de este dispositivo se considera Indicación Clase IIb Nivel de evidencia C. (5)
En este paciente se realizó ecocardiograma y se descartó patología estructural, así como disfunción ventricular; el intervalo QTc fue normal, sin embargo, la frecuencia cardiaca fue de 42 lpm por lo que se implantó marcapasos.
En cuanto a la ubicación del electrodo, así como al modo de estimulación, se ha demostrado que la estimulación modo VVI con electrodo en ventrículo izquierdo ha resultado eficaz en cuanto a prevenir la disincronía en el seguimiento, por lo que se aplicó este protocolo en el paciente presentado. (5)
Referencias
- Morquio L. Sur une maladie infantile et familiale caractérisée par des modifications permanentes du pouls, des attaques syncopales et epileptiforme et la mort subite. Archives médicales d'enfants. 1901;4:467.
- Tunaoglu FS, Yildirim A, Vurali D. Isolated congenital heart block. Texas Heart Institute Journal. 2010;37:579-583.
- Schmidt K, Ulmer H, Silverman N, Kleinman C, Copel J. Perinatal outcome of fetal complete atrioventricular block: a multicenter experience. J Am Coll Cardiol. 1991;17:1360-1366.
- Dunn H. Antenatal diagnosis of congenital heart block. J Obstet Gynaecol Br Empire. 1960;67:1006-1007.
- Brignole M, Auricchio A, Barón Esquivias G, Bordachar P, Boriani G, Breithardt OA, et al. Guía de práctica clínica de la ESC 2013 sobre estimulación cardiaca y terapia de resincronización cardiaca. Rev Esp Cardiol. 2014;67:e1-e60.
- Begoña B. Muerte súbita en pacientes sin cardiopatía estructural. Rev Esp Cardiol Supl. 2013;13:14-23.
- Bordachar P, Whinnett Z, Ploux S, Labrousse L, Haissaguerre M, Thambo JB. Pathophysiology, clinical course, and management og congenital complete atrioventricular block. Heart Rhythm. 2013;10:760-766.
- Josephson M. Atrioventricular conduction. In Josephson M, editor. Clinical cardiac electrophysiology. Cuarta ed. Philadelphia: Lippincott Williams & Wilkins; 2008. p. 93-113.
- Fisch C, Knoebel S. Atrioventricular and ventriculoatrial conduction and blocks, gap, and overdrive suppression. In Fisch C, Knoebel S, editors. Electrocardiography of clinical arrhythmias. Armonk, NY: Futura; 2000. p. 315-344.
- Abrams DJ, MacRae CA. Long QT syndrome. Circulation. 2014;129:1524-1529.
|

