Introducción
La apendicitis aguda (AA) es la primera causa de cirugía en pediatría, cuya incidencia es máxima entre los 10 y 12 años(1). Es de manejo urgente, con una tasa de morbilidad directamente proporcional al tiempo transcurrido entre su inicio y la resolución quirúrgica definitiva(1).
Es causada por inflamación del apéndice vermiforme, originada por obstrucción de su lumen. Puede deberse a inflamación de los folículos linfoides, fecalitos, parásitos y estrechez por tumoración o fibrosis(1,2).
El cuadro clínico clásico de la AA corresponde a dolor epigástrico o periumbilical inicial que migra a fosa ilíaca derecha (FID), asociado a fiebre de baja cuantía, anorexia, náuseas y vómito. Por otra parte, se estima que el porcentaje de presentación atípica de una AA está alrededor del 37%, siendo mayor en la población masculina, con una relación 2:1(3). El síntoma atípico más frecuente es la diarrea, seguido de dolor abdominal que no muestra un curso o localización clásica (alrededor de 17%)(4).
La AA de presentación atípica puede sobreponerse con otros síndromes clínicos y asociarse con significativa morbilidad, que se incrementa con el retraso diagnóstico(1,5). Como complicación de la AA se puede producir una perforación del órgano, llevando a un proceso inflamatorio local denominado plastrón apendicular, que puede evolucionar a la abscedación. Éste se presenta en el 2-6% de los casos de AA(6). Al examen físico se presenta como masa palpable en FID, con o sin dolor.
Presentamos a continuación un caso clínico de un paciente pre-adolescente con un cuadro de AA asociado a masa abdominal palpable en FID.
Caso Clínico
Paciente D.C.C., de 11 años de edad. Antecedente de prematurez, hiperreactividad bronquial y constipación crónica, con múltiples consultas en Servicio de Urgencia Infantil (SUI) para enemas evacuantes.
Acude nuevamente a SUI, presentando cuadro de 12 horas de evolución de dolor abdominal en región periumbilical de inicio brusco, tipo cólico, en relación a transgresión alimentaria, que no cede con antiespasmódicos. Asoció un vómito alimentario y un episodio diarreico, sin elementos patológicos.
Ante persistencia de dolor abdominal y asociación con fiebre de baja cuantía (hasta 38ºC), consulta 2 días después del inicio del cuadro en SUI del Hospital Exequiel González Cortés (HEGC).
Al examen físico por Cirujano Infantil se constata abdomen blando y depresible, con masa palpable en FID, levemente dolorosa. No presenta resistencia muscular ni signos de irritación peritoneal.
Cuenta con reciente estudio imagenológico, solicitado en su última asistencia a SUI:
- Ecotomografía abdominal: órganos intraabdominales de tamaño, situación y ecoestructura conservados. Sin apreciación de líquido libre. Significativa cantidad de material estercoráceo intestinal en hemiabdomen inferior.
- Radiografía de abdomen simple concordante.
Por antecedente de constipación crónica, se realiza enema evacuante, solicitándose posteriormente exámenes de laboratorio e imagenológicos:
- Perfil hematológico: leucocitos: 9.400/mm3
- PCR: 0.4 mg/dl
- Radiografía de abdomen simple: imagen concordante con abundantes deposiciones en intestino grueso.
Al reexaminar tras realización de enema evacuante, se aprecia persistencia de masa en FID, sin variaciones. Se decide por tanto ingreso hospitalario para estudio y observación clínica, indicándose régimen cero y fleboclisis.
Equipo de Cirugía Infantil plantea mayor estudio de masa abdominal, por lo que se solicitan nuevos exámenes de laboratorio y ecografía abdominal.
Ecotomografía abdominal: apéndice cecal engrosado de 1 cm. no compresible con el transductor, con moderada cantidad de líquido libre local. Adenopatías mesentéricas vecinas de ecoestructura conservada. Paredes de colon ascendente vecino algo engrosadas. Resto de abdomen normal. Diagnóstico ecográfico: apendicitis aguda en evolución.
Con clínica descrita y exámenes imagenológicos, se decide resolución quirúrgica del cuadro e inicio de antibioprofilaxis endovenosa.
Protocolo Operatorio
Diagnóstico pre-operatorio: masa abdominal FID en estudio, apendicitis aguda en evolución por ecografía.
Se aborda con laparotomía Mc Burney. Abierto peritoneo, se visualiza líquido citrino y dilatación cecal con paredes congestivas. Se realiza exploración manual y se palpa masa semisólida irregular móvil dentro del ciego que impresiona como acumulación estercorácea. Se identifica apéndice cecal congestivo, con base ancha, sin fibrina ni necrosis. Se ligan
meso más base apendicular y seccionan los mismos.
Diagnóstico post-operatorio: apendicitis aguda grado I, fecaloma cecal.
El paciente evoluciona satisfactoriamente, con realimentación a las 12 hrs post-cirugía y buena respuesta a analgésicos. Se decide alta a las 48 hrs.
Biopsia apéndice vermiforme:
Discusión
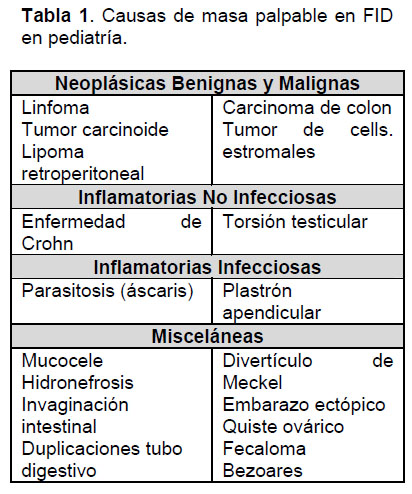
Si bien la asociación de masa abdominal en FID y clínica compatible con AA es baja(6), esto tiene implicancia directa en el manejo. La orientación diagnostica de masa en FID, con o sin dolor abdominal local, debe considerar neoplasias benignas y malignas, procesos inflamatorios infecciosos y no infecciosos, y otras causas menos frecuentes(7,8,9).
En líneas generales, hay 4 abordajes posibles en esta situación, cuando el origen apendicular de la masa no es obvio(10,11,12):
- Laparotomía inmediata con intención de apendicectomía
- Ventaja: evita rehospitalización para apendicectomía, exclusión de patologías enmascaradas que se presentan como masa en FID.
- Desventaja: complicaciones post-operatorias más frecuentes, mayor tiempo de hospitalización.
- Laparotomía diferida con intención de apendicectomía
- Ventaja: evita recurrencia de síntomas, evita diagnóstico erróneo de masa en FID atribuida al apéndice, operación menos dificultosa.
- Desventaja: rehospitalización para apendicectomía.
- Drenaje percutáneo guiado por TC o ecografía
- Ventaja: permite drenaje de pus y cultivo bacteriano, resolución proceso inflamatorio, evita cirugía mayor.
- Desventaja: operador-dependiente, requiere asociación con método imagenológico como guía, alto costo, sin amplia disponibilidad.
- Manejo conservador (antibioterapia)
- Ventaja: no someter al riesgo quirúrgico.
- Desventaja: no diagnosticar tumor de apéndice o colónico, posibilidad de recurrencia de síntomas, dificultad en exclusión de otras patologías.
 |
Es sabido que en niños y adolescentes es más difícil lograr el diagnóstico correcto de AA, dado que su presentación inicial puede ser solapada o imitada por otras condiciones también comunes(13,14). El retraso en el diagnóstico de la AA incrementa el riesgo de perforación, lo que se asocia a complicaciones post-quirúrgicas que pueden llegar hasta el 40%(5).
Si bien la ecografía abdominal puede tener una alta sensibilidad y especificidad en el diagnóstico de AA, no se puede generalizar un protocolo para centros médicos terciarios. El diagnóstico radiográfico de AA en pediatría es altamente operador-dependiente, con una variación de 70 – 95% en especificidad(15,16).
Usualmente se deja en observación a los pacientes con signos y síntomas sospechosos de AA para aumentar la especificidad del diagnóstico preoperatorio. Sin embargo, este tiempo de espera puede incrementar la tasa de perforación y sus complicaciones asociadas(16). En consecuencia, se hace primordial el diagnóstico rápido en el paciente pediátrico con AA.
En nuestro caso, la masa en FID podría haber conducido erróneamente al diagnóstico de plastrón apendicular. Sin embargo, considerando el antecedente de constipación crónica y la persistencia de la masa tras enema evacuante, se decidió proceder con cirugía, ante la eventualidad de que la AA fuese inicial más que avanzada en su evolución natural.
Conclusión
El cirujano infantil debe evaluar a un gran número de pacientes que se presentan al SUI con dolor abdominal como motivo de consulta. El acercamiento diagnostico debe ser distinto cuando hay masa abdominal en FID, debiendo ampliar las posibilidades etiológicas e investigar el caso cuidadosamente, con un detallado análisis de la historia clínica, laboratorio e imagenología si está disponible.
Si el diagnóstico de abdomen agudo sigue siendo dudoso tras un tiempo prudente de observación y se está aún en presencia de masa en FID, la intervención quirúrgica inmediata es una opción viable según el nivel de experticia del cirujano, dado su rol diagnóstico y terapéutico. No se debe olvidar que la meta del cirujano es minimizar la tasa de apendicectomías negativas sin incrementar la incidencia de perforación, mientras exista el riesgo de que esto suceda.
Referencias
- Bundy D., Byerley J.., Liles A. “Does this child have appendicitis?” JAMA 2007; 298(4): 438-451.
- Rothrock SG, Pagane J. “Acute appendicitis in children: emergency department diagnosis and management”. Ann Emerg Med. Jul 2000;36(1):39-51.
- Becker T, Kharbanda A, Bachur R. “Atypical clinical features of pediatric apendicitis”. Acad Emerg Med. Feb 2007;14(2):124-9.
- Beltrán M., Villar R., Tapia T., Cruce K. “Sintomatología atípica en 140 pacientes con apendicitis”. Rev Chil Cir 2004; 56: 269-74.
- Mueller BA, Daling JR, Moore DE, et al. “Appendectomy and risk of tubal infertility”. N Engl J Med. 1986;315:1506–1508.
- Nitecki, S., Assalia, A. and Schein, M. (1993), “Contemporary management of the appendiceal mass”. British Journal of Surgery, 80: 18–20.
- Hazuková R, Rejchrt S, Vacek Z, Kopáčová M, Dvořák P, Bureš J. “Pitfalls of palpable mass in the right iliac fossa. Report of two cases of chronic absceding appendicitis”. Folia Gastroenterol Hepatol 2005; 3 (3): 99 – 103.
- Marshall M., Rosen P., Berlin R., Greenson N. “Appendicitis masquerading as tumor: a case of two diagnosis”. J Emerg Med. 2001 Nov;21(4):397-9.
- Villamartín M. “Complicaciones quirúrgicas de la infestación por áscaris”. En: Cirugía Pediátrica. Cap. 43, p. 346-53. 1994.
- J S Jordan, P J Kovalcik, C W Schwab. “Appendicitis with a palpable mass”. Ann Surg. 1981 Feb.; 193(2): 227–229.
- Garba E., Ahmed A. “Management of appendiceal mass”. Annals of African Medicine, Vol. 7, No.4; 2008: 200 – 204.
- Okune E., Marek G., Jarosław K. “Management of appendiceal mass in children and adults: our experience”. The Internet Journal of Surgery. 2007 Vol. 9, No. 2.
- Balibrea JL. “Diagnóstico diferencial del abdomen agudo”. En: Urgencias Médico-Quirúrgicas. Edit. Universidad Autónoma de Barcelona, J. Uriach & Cia; 1990. p. 65-96.
- Gamal R, Moore TC. “Appendicitis in children aged 13 years and younger”. Am J Surg. 1990;159:589–592.
- Lee SL, Ho HS. “Ultrasonography and computed tomography in suspected acute appendicitis”. Semin Ultrasound CT MR 2003; 24: 69-73.
- García B., Taylor G., Fishman S. “Effect of an imaging protocol on clinical outcomes among pediatric patients with appendicitis”. Pediatrics 2002;110;1088.
|

